Dùng khí hiđro để khử hết 50g hỗn hợp A gồm đồng(II)oxit và sắt(III)oxit. Biết trong hỗn hợp sắt(III)oxit chiếm 80% khối lượng.
a) Tính khối lượng mỗi chất trong hỗn hợp
b) Tính thể tích hiđro (đktc) đã dùng
c) Tính khối lượng kim loại đồng sắt thu được





























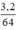 = 0,05 mol
= 0,05 mol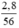 = 0,05 (mol)
= 0,05 (mol)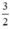 . n
. n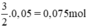 ⇒ V
⇒ V